
A fragmentaçăo por captura de elétrons (Electron Capture Dissociation – ECD) é um dos métodos de fragmentaçăo que podem ser aplicados em MS/MS (Espectrometria de massas sequencial) e consiste na introduçăo de um elétron de baixa energia (cerca de 0,2 eV) no íon em fase gasosa.
A fragmentaçăo em MS/MS pode ser realizada por diversas técnicas, entre elas o processo de dissociaçăo induzida por colisăo (CID), o processo de dissociaçăo por captura de elétrons (ECD), dissociaçăo induzida por radiaçăo multifotônica no infravermelho (IRMPD), entre outros. Devido ŕs diferenças entre os mecanismo e fragmentaçăo, essas técnicas normalmente săo aplicadas em tipos distintos de moléculas.
A fragmentaçăo ECD é majoritariamente introduzida no estudo de peptídeos por apresentar a característica de produzir fragmentos c e z , enquanto em técnicas como o CID, os fragmentos produzidos săo majoritariamente b e y.
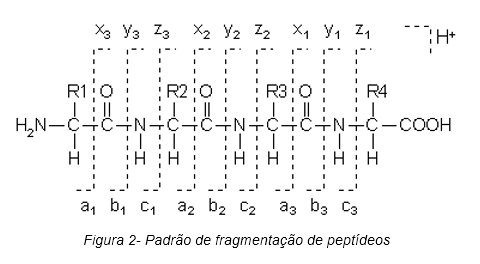
A principal diferença entre esses fragmentos está relacionada com a estabilidade da ligaçăo na qual ocorre a clivagem, no caso do fragmentos b e y, a clivagem é puramente termodinâmica e pode ocorrer com o simples aumento de energia do sistema.
Diferentemente dos fragmentos b e y, os fragmentos c e z produzidos pela fragmentaçăo ECD năo săo provenientes de uma clivagem termodinâmica, indicando a participaçăo orbitalar nesse mecanismo. O mecanismo de fragmentaçăo ECD ainda é excessivamente discutido, sendo o modelo mais aceito o de Washington-Utah. Nesse mecanismo, entretanto, ainda existem duas possibilidades: two-step e one-step.
Two-Step
Nessa versăo do modelo WU, o elétron é capturado por um orbital de Rydberg localizado em um sítio positivamente carregado e posteriormente transferido para um orbital π* da amina (na backbone do peptídeo) que seja favorável ŕ receber esse elétron, ou seja, que possua uma estabilizaçăo maior que 2.0 eV. Entretanto, como para que essa transferęncia ocorra é necessária a remoçăo do elétron do orbital de Rydberg onde ele está instalado, é necessário que a energia de estabilizaçăo do orbital π* que receberá o elétron seja de 2.0 eV mais a energia de estabilizaçăo do elétron associado ao orbital de Rydberg, para que a remoçăo do elétron seja possível.
One-Step
Essa alternativa propőe que, diferentemente do modelo Two-Step, o elétron năo se ligue ao orbital de Rydberg localizado em um sítio positivamente carregado. Nessa versăo o orbital de Rydberg agiria apenas guiando o elétron (por meio de sobreposiçăo orbitalar) ao orbital π* da amida, sem que o elétron se ligue ŕ ele. Como consequęncia, a estabilizaçăo do orbital π* que receberá o elétron năo precisa superar o extra de energia de estabilizaçăo do elétron no orbital de Rydberg, uma vez que essa ligaçăo năo ocorre.
Uma vez que o elétron está ligado ao orbital π* da amida, a clivagem N-Cα pode ocorrer superando a barreira energética que é muito menor do que a barreira para a clivagem homolítica dessa ligaçăo na ausęncia do elétron. É importante ressaltar que a estabilizaçăo dos orbitais π* é devido ŕs forças Coulombicas e elestrostáticas no sítio que a ligaçăo N-Cα se encontra.
Sendo a clivagem por ECD uma fragmentaçăo năo-energótica e năo-termodinâmica, as cadeias laterais e modificaçőes (fosforilaçőes, metilaçőes e etc) permanecem intactas - năo săo clivadas, sendo essa uma das maiores vantagens da fragmentaçăo ECD por permitir a identificaçăo de modificaçőes pós-traducionais em proteínas.
[1] Zubarev, R., Kelleher, N. L., & McLafferty, F. W. (1998). Electron capture dissociation of multiply charged protein cations. A …. J. Am. Chem. Soc, 120(16), 3265–3266. http://doi.org/10.1021/ja973478k [2] Kruger, N. A., Zubarev, R. A., Horn, D. M., & McLafferty, F. W. (1999). Electron capture dissociation of multiply charged peptide cations. International Journal of Mass Spectrometry, 185-187(July 1998), 787–793. http://doi.org/10.1016/S1387-3806(98)14215-X