CurTiPot=
Programa para Cálculo de pH
|
||||||||||||||||||
|
|
CurTiPot 4.4.0 * |
|
|
Programa completo
com primeiros passos para iniciantes ** |
||
|
Programa completo
|
||
|
Programa completo
zipado |
||
|
* Requer Microsoft ExcelTM
- versão 12 (2007) em diante.
|
||
>200 mil cópias de
CurTiPot distribuídas em > 100
países.
Downloads para >200 universidades e
centenas de empresas (dados do
Google Analytics).
CurTiPot é usado no ensino, pesquisa e laboratórios de
análise.
>300 usos e citações de CurTiPot em publicações
e teses.
Numa valiação de 21
aplicativos e calculadoras de pH,
somente dois deram resultados corretos e o uso de
CurTiPot é encorajado frente a todos os demais para
cálculos rigorosos e confiávies de pH.
Lucy, C. L., J. Chem. Educ. 2023, 100, 2418−2422
doi.org/10.1021/acs.jchemed.2c01203
Você pode citar o CurTiPot
assim:
Gutz, I. G. R., programa CurTiPot - pH e
Curvas de Titulação Potenciométrica:
Análise e Simulação, versão 4.4.0,
https://www.iq.usp.br/gutz/Curtipot.html
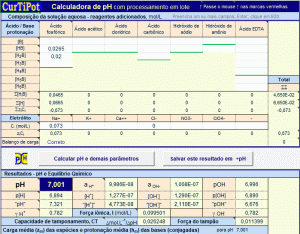
cálculos de pH - de soluções aquosas de ácidos, bases e sais, simples ou complexas (>30 espécies), incluindo tampões e aminoácidos, com avaliação de força iônica, coeficientes de atividade, distribuição das espécies (frações molares), carga média, indicação de Ponto Isoelétrico e capacidade de tamponamento (poder tampão e capacidade tamponante); os cálculos de pH são feitos por meio de uma equação geral completa no lugar da equação aproximada de Henderson-Hasselbalch.
análise de dados de pH vs. volume de titulações potenciométricas reais ou simuladas:
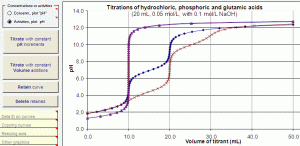
» representação gráfica de curvas de titulação ácido-base, suas derivadas e distribuição das espécies;
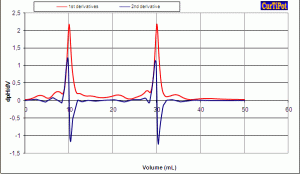
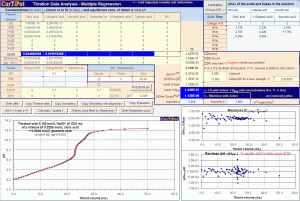
» tratamento de dados automático, com localização precisa das inflexões (pontos finais) nas curvas das derivadas (1a e 2a) assistida por interpolação com alisamento por splines cúbicos (módulo Analise_I);
» determinação de múltiplas concentrações e refinamento de valores de pKa por regressão não linear múltipla (módulo Analise_II); essencial para amostras muito diluídas ou complexas, cujas curvas de titulação apresentam inflexões pouco definidas, p. ex., chuva ácida;
» todos os resultados de interesse podem ser salvos (com identificação e dados respectivos) para uso posterior;
» Processamento em lote disponível para cálculo de pH e parâmetros selecionados de longas listas de soluções com composição variável de ácidos e bases.
Titulador Virtual e Simulador de curvas de titulação ácido-base;
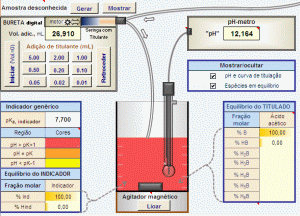
» Titulador virtual para estudantes, com bureta digital clicável e indicação de ponto final por transição de cor de indicador ácido-base; curva de pH vs. volume de titulante opcional; geração opcional de "amostras desconhecidas";
» Simulador de curvas de titulação (pH ou "pH" vs. volume de titulante) de soluções aquosas com ácidos, bases, sais, tampões ou mesmo misturas com dezenas de espécies;
» simulação de erros experimentais aleatórios no pH e/ou no volume das adiçõe de titulante, para avaliação do efeito na exatidão do tratamento de dados (nos módulos Análise I e Análise II);
» incrementos selecionáveis de pH ou de volume e sobreposição gráfica de até 14 curvas para comparação do efeito vários parâmetros;
» sobreposição de curva de titulação com dados reais e simuladas para variação dos parâmetros até haver ajuste (pode ser feito automaticamente em Análise II);
» geração de número ilimitado de curvas de titulação distintas para uso como exercícios e em exames de alunos.
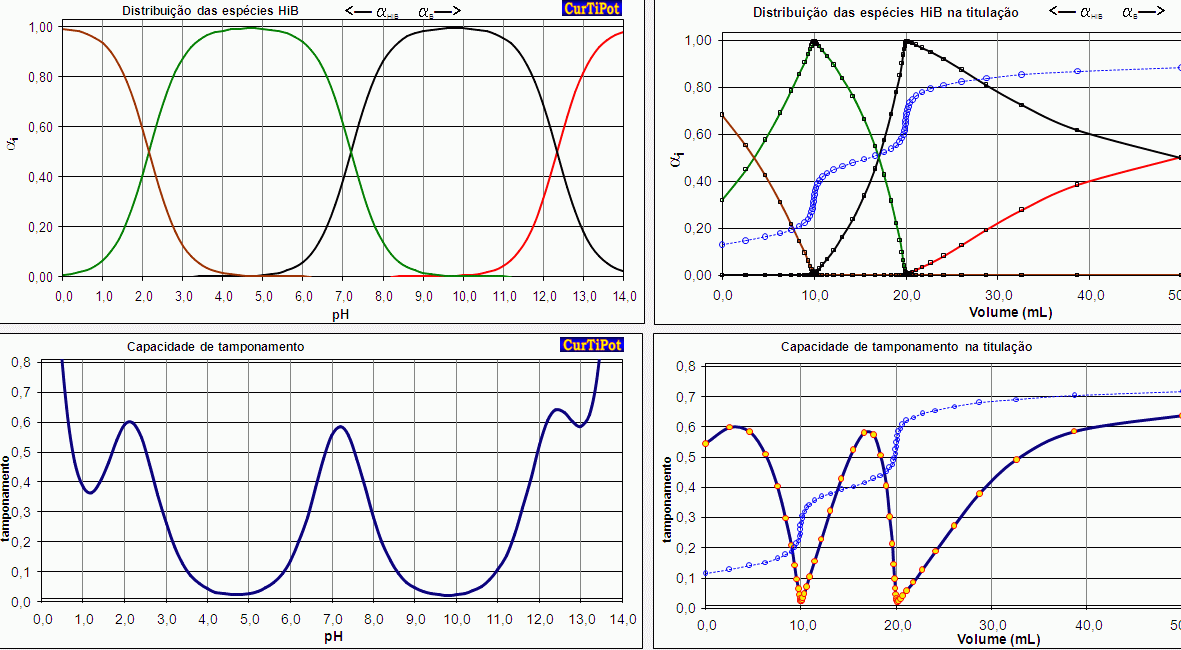
Geração de diagramas de protonação, capacidade de tamponamento, distribuição das espécies, curvas de Bjerrum e carga média, revelando as regiões de predominância de cada forma (protonada ou desprotonada) tanto em função do pH como do volume de titulante adicionado, em escala linear e logarítmica, e localizando o Ponto Isoelétrico (se houver).
CurTiPot é distribuído gratuitamente (freeware) nesta página <www.iq.usp.br/gutz/Curtipot.html> para uso pessoal, educacional e não comercial; para outras aplicações, consultar o autor (detentor dos direitos autorais).
Não é necessário instalar ou desinstalar o programa CurTiPot. Basta abrir o arquivo como qualquer outra planilha Excel em computadores com o Office da Microsoft instalado, para visualizar todas as planilhas. Para realizar cálculos com as macros pré-programadas em Visual Basic for Applications, é necessário habilitar a planilha primeiro.
Instruções para habilitar as macros nas versões mais recentes do Windows:
1. Baixe o arquivo CurTiPot desta página/site do autor para um folder da sua preferência no seu computador;
2. Abra o folder e clique com o botão direito no arquivo curtipot.xlm;
3. Escolha "Propriedades" na janela que se abrir;
4. Assinale "desbloquear" (em geral, próximo ao canto inferior direito);
5. Clique OK;
6. Dê um clique duplo no arquivo curtipot_.xlm para abrí-lo;
7. Escolha "Habilitar conteúdo", se a pregunta aparecer na barra de segurança;
8. Siga as instruções nas planilhas do CurTiPot.
Os procedimentos de habilitação para algumas versões antigas do Windows estão descritos na primeira página do CuTiPot (que pode ser lida sem habilitação).
Todas as células com marca vermelha no canto superior direito contêm instruções de uso, informações e/ou comentários; para consultá-los, basta apontá-las com o mouse (e, dependendo da versão do Excel, clicar no botão direito e escolher Mostrar).
CurTiPot opção i para iniciantes tem, adicionalmente, balões (descartáveis) indicando a sequência elementar de passos a seguir.
O módulo de Análise_II permite determinar concentrações e pKas por regressão não linear de mínimos quadrados por meio do Solver, um suplemento que acompanha o Excel no pacote Office da Microsoft. Aparece à direita no menu Dados (no Excel antigo, em Ferramentas); se estiver ausente, adicioná-lo em Arquivo / Opções do Excel / Suplementos / Solver.
A versão de CurTiPot em arquivo .xlsm aqui distribuída se mostrou compatível com todas as versões do Excel testadas a partir de 2007. Favor reportar problemas ao autor ou se a única versão de Excel disponível for anterior a 2007, solicitar cópia em formato .xls.
O programa considera somente equilíbrios (rápidos) de protonação e desprotonação de bases e ácidos (segundo o conceito de Brönsted e Lowry), ignorando outras reações químicas, equilíbrios de fase e aspectos cinéticos.
Os módulos pH, Simulador, Distribuição e Análise II levam em conta os efeitos da força iônica do meio. Os coeficientes de atividade* são estimados pela equação de Davies**.
Para determinar não só as concentrações dos analitos titulados mas também refinar os valores das constantes de dissociação, pKa, no módulo Análise_II, os dados experimentais potenciométricos obtidos com um pH-metro (peagômetro) devem ser isentos de erros de calibração e desvios de linearidade do sensor. Eventuais efeitos de erro alcalino do eletrodo de vidro combinado ou de variação do potencial de junção devem ser corrigidos (descontados) previamente.
O autor cede o programa gratuitamente "no estado em que se encontra" para uso educacional e não comercial, sem qualquer garantia expressa ou implícita de exatidão dos resultados, do funcionamento correto em qualquer situação e dos valores de pKa compilados. O autor não assume responsabilidade por consequências decorrentes do uso dos resultados.
Notificações de erro e sugestões são bem vindas pelo e-mail gutz@iq.usp.br.
* No ensino médio, costuma-se definir pH como -log [H+], ignorando as interações iônicas que ocorrem em solução. Pode-se dizer que esta expressão fornece o p[H] ou o "p[H]" pois, pela definição da IUPAC (veja definição de pH), o pH corresponde a -log a[H+] onde a[H+] é a atividade do íon H+, ou seja, [H+] x coef. de atividade. Os pontos finais (ou pontos estequiométricos) de curvas de titulação independem de se usar pH, p[H] ou "[pH]", vez que os pequenos deslocamentos no eixo das ordenadas não mudam a posição das inflexões sobre o eixo das abcissas. Contudo, ao calcular o pH de uma solução (p.ex., um tampão), a diferença entre usar -log [H+] ou -log a[H+] pode ser grande.
** Há versões estendidas da equação de Debye-Hückel que permitem reduzir a incerteza dos valores calculados com a equação de Davies em foça iônica elevada, desde que se conheça a dimensão efetiva de cada íon hidratado e as constantes de associação entre íons diferentes, parâmetros nem sempre disponíveis para os ácidos e bases de interesse.
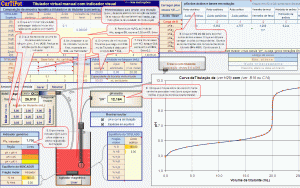
A organização modular, amigável e interativa do programa permite que você simule rapidamente novas titulações escolhendo os componentes, suas concentrações, os incrementos e a rapidez das adições, os volumes e a dispersão dos dados. Com um simples clique, os dados simulados são copiados para os módulos de análise por método gráfico e/ou numérico. Isso é ótimo tanto no ensino como em estudos de viabilidade e definição de condições de trabalho de novas titulações.
Você se surpreenderá com a eficiência da interpolação com alisamento do módulo de Análise I para titulações do grupo a) e com o poder do ajuste por regressão da Analise II para titulações difíceis do grupo b) abaixo.
a) Titulações volumétricas com inflexões bem definidas.
Digite os pares de dados experimentais obtidos no laboratório diretamente na planilha de Análise Inicial enquanto faz a titulação manualmente, ou transfira os dados do titulador automático após o término da titulação. Selecione a intensidade do alisamento (suavização) entre 0 (mínimo) e 100 (máximo), de forma a conseguir a interpolação mais precisa do(s) ponto(s) de inflexão (ponto estequiométrico ou ponto de equivalência), observável como um máximo ou um mínimo na derivada primeira da curva.b) Curvas com inflexões indefinidas ou sobrepostas.
O módulo Análise_II permite determinar concentrações e refinar pKas mesmo para certas curvas intratáveis por métodos gráficos e de linearização (como o de Gran). O recurso quimiométrico de ajuste por mínimos quadrados funciona melhor quando todos os pKas relevantes se situam dentro da faixa de pH abrangida pelos dados. Noções de quimiometria, estatística ou análise numérica não são essenciais, mas se você as tiver, aprenderá mais rapidamente a explorar os recursos deste módulo e a reconhecer seu poder e suas limitações (ele não faz milagre com dados inadequados!).Por exemplo, concentrações mínimas (traços) de alguns ácidos e báses presentes na chuva ácida podem ser determinados por titulação, individualmente ou agrupados como segue: ácidos fortes (H2SO4 + HNO3), ácidos carboxílicos fracos (fórmico + acético), bicarbonato (H2CO3/HCO3-/CO3=) e amônio (NH4+/NH3) (FORNARO, A.; GUTZ, I.G.R., Wet deposition and related atmospheric chemistry in the São Paulo metropolis, Brazil. Part 3: Trends in precipitation chemistry during 19832003, Atmospheric Environment, 2006, 40(30), 5893-5901).
Em princípio, tanto o Titulador como o Simulador do CurTiPot pode ser usado para gerar qualquer curva de titulação em meio aquoso, independentemente do número e concentração de sistemas ácido-base em equilíbrio (dentro das limitações dadas acima), inclusive as mais simples e comuns: ácido forte - base forte; ácido fraco - base forte; ácido forte - base fraca; e ácido fraco - base fraca. No Titulador as adições são feitas manualmente, ponto a ponto, sendo exibida a viragem de um indicador e, opcionalmente, a distribuição das espécies e a curva de "pH" vs. volume. Já o Simulador gera automaticamente curvas completas, trabalha em pH e "pH" e tem mais recursos.
O programa é usado frequentemente para simular titulações de aminoácidos (dipróticos e tripróticos), ou de outros sistemas polipróticos. Inspeção do correspondente diagrama de distribuição de espécies e de carga média permite localizar o ponto isoelétrico, o que também é feito automaticamente. Outra aplicação interessante é a do estudo do efeito de absorção de CO2 (gás carbônico) do ar sobre o pH de soluções e titulações.
Em nosso laboratório, usamos CurTiPot, p. ex., para simular e fornecer valores calculados de pH vs. volume de titulante em um método de análise de dados de titulações condutométricas (COELHO, L.H.G. and GUTZ, I.G.R., Trace analysis of acids and bases by conductometric titration with multiparametric non-linear regression, Talanta, 2006, 69(1), 204-209).
O programa também é útil para tarefas como determinar a quantidade de ácido ou base necessária para a neutralização de uma amostra, para observar a resistência de uma solução tampão à adição de ácido ou de base (calcula a capacidade tamponante), para avaliar a transição de cor de indicadores visuais, para revelar o ponto isoelétrico de aminoácidos, etc.
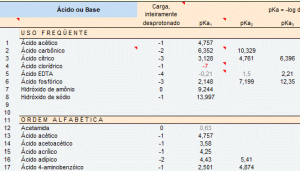
A base de dados do programa CurTipot traz os pKas de cerca de 250 ácidos e bases monopróticos, dipróticos e polipróticos mais comuns, incluindo aminoácidos e exemplos de indicadorese, e cada um pode acrescentar os pKas das substâncias do seu interesse.
|
||
|
Descrição | Download
| Telas | Instalação
Algumas Citações e Apreciações
Agência FAPESP | Testemunhos
| >200 mil cópias distribuídas em >100
países; Visitas registradas pelo Google Analytics e contadas pelo Statcounter (português + inglês a partir de 2006) Distribuição
por país e estado/cidade Exemplo de distribuição por país 
Vídeos - Tutoriais - CurTiPot
Química dos ácidos e bases (16:03) Fundamentos da Titulação (9:18) Titulação e Tampões (12:39) pH e pKa (18:11); Espontaneidade (20:04) Eletrodo de vidro, funcionamento e calibração (animação 3D, 5 min, Chemical Lab) Potenciometria com eletrodo de vidro (29 min. Prof. Ivano Gutz, IQ-USP); titulações (introdução) (10 min) Potenciometria com eletrodo de vidro (16 min, Prof. Thiago Paixão, IQ-USP) 1 - Calibração dos eletrodos (13:06) 2 - Medições de pH e condutividade (5:01) 3 - Titulação de Vitamina C (7:36) 4 - Titulação de Paracetamol (6:36) 5 - Tratamento de dados de titulação potenciométrica com CurTiPot (20:00) 6 Tratamento
de dados de titulação condutométrica com
CurTiPot-Cond* (5:06) CurTiPot - Playlist com 5 partes |